Resumen
En la naturaleza existen distintos tipos de sólidos que pueden ser estudiados desde su estructura atómica para interpretar las propiedades que los identifican. La comprensión de los átomos y la estructura que los compone es útil para analizar lo que sucede en el interior de los materiales y explicar algunas propiedades como la conductividad. Una de las partículas subatómicas de mayor importancia es el electrón, ya que, a partir de la comprensión del comportamiento de los electrones, se puede entender la generación de enlaces entre elementos en relación con los niveles de energía que presenta, los cuales se combinan en bandas de energía, siendo la banda de valencia y la banda de conducción elementos importantes para la comprensión del comportamiento conductivo de los materiales. La implementación de los diagramas de bandas de energía son recursos visuales que son útiles para comprender el comportamiento de los electrones en los materiales y asimilar la diferencia que existe entre los metales, los aislantes y los semiconductores.
Palabras clave: electrones, conductividad, energía
En la naturaleza de los materiales existen muchas variedades de sólidos con características y propiedades diferentes. Los metales son como autopistas abiertas que dejan pasar la corriente sin resistencia; los aislantes, se comportan como muros que bloquean el paso de la electricidad, y existen también los semiconductores, curiosos materiales capaces de actuar como conductores o como aislantes, según las condiciones en que se encuentren.
Sabias que… hay una disciplina científica especializada en el estudio de la estructura, las propiedades y el procesamiento de los materiales llamada ciencia de materiales, es una ciencia multidisciplinaria que integra conocimientos de física, química y matemáticas que tiene la finalidad de entender y manipular la materia a nivel atómico y molecular.
La clave está en los electrones
La mayoría de las propiedades de los sólidos pueden ser explicadas por el comportamiento de sus electrones en relación con la forman en la que se encuentran organizados dentro de los materiales y, sobre todo, en la interacción de los átomos en el interior del sólido; una de estas propiedades es la conductividad, la cual puede ser comprendida como la habilidad que tiene un objeto de conducir corriente eléctrica. La comprensión de la electricidad ha sido un proceso gradual desarrollado a lo largo de varios años con contribuciones de renombrados científicos como Tales de Mileto, Benjamin Franklin, Michael Faraday y Nikola Tesla entre muchos otros.
Para entender realmente cómo funciona un material necesitamos mirar a sus piezas más pequeñas: los átomos; de acuerdo con la teoría atómica de Bohr, los átomos tienen una estructura basada en un núcleo formado por protones con carga positiva y neutrones con carga neutra. Alrededor de este núcleo, se encuentran los electrones con carga negativa posicionados en orbitales, los cuales se distribuyen en niveles de energía, como si fueran los pisos de un edificio.
Los electrones se posicionan primero en los orbitales de menor energía y siguen un orden específico para pasar hacia los de mayor energía; para determinar el llenado de los orbitales, se utiliza como recurso el diagrama de Moeller:
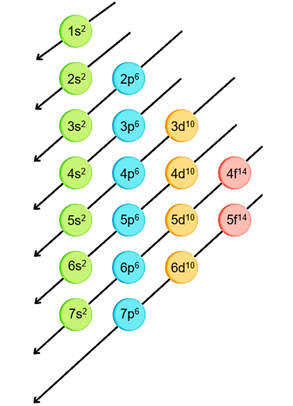
Cada nivel está representado por un número asignado llamado número cuántico principal “n”, el cual inicial en el nivel 1 y aumenta en unanimidad. Dentro de cada nivel se generan divisiones más pequeñas llamadas subniveles que son orbitales con distintas formas, los cuales se denominan s, p, d y f.
En la tabla periódica, los elementos están ordenados de acuerdo con su número atómico, el cual indica el número de protones presentes en el núcleo del átomo, y de manera indirecta, también indica el número de electrones, debido a que la carga del átomo es considerada neutra, por lo tanto, el número de electrones y protones es el mismo; el número atómico es imprescindible para obtener la configuración electrónica del átomo, la cual describirá la distribución de electrones dentro de un átomo.
El caso del silicio, la arena que cambió al mundo
El silicio es el segundo elemento más abundante en la corteza terrestre (después del oxígeno), ya que puede encontrarse en la arena de playa, sin embargo, el que se utiliza en la industria de los chips no proviene directamente de esta fuente, ya que necesita someterse a un proceso de purificación tan extremo que el silicio final alcanza una pureza superior al 99.9999%.
Desde que se inventó el primer transistor en 1947, el silicio es un semiconductor por excelencia que ha protagonizado una revolución tecnológica. En la actualidad, en un chip del tamaño de una uña, pueden convivir más de 10 mil millones de transistores, todos hechos con este material.
El silicio tiene el número atómico 14, por lo tanto, cuenta con 14 protones y 14 electrones que deben ser organizados en relación con su configuración electrónica:
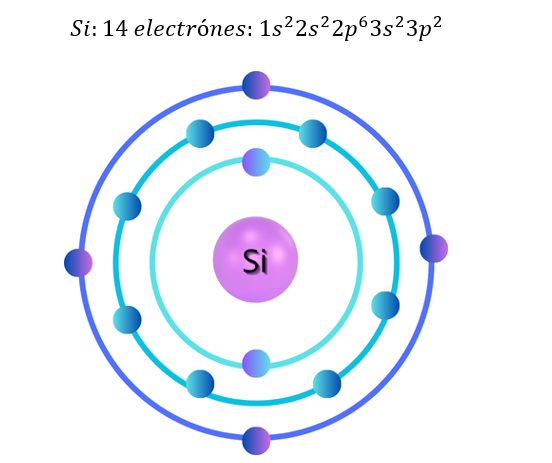
Una de las partes más importantes de la configuración electrónica es el último nivel de energía; los electrones presentes en el último nivel se denominan electrones de valencia y son los responsables de la generación de enlaces entre elementos para la formación de moléculas mediante la creación de orbitales moleculares. El silicio tiene cuatro electrones de valencia que son los responsables de la generación de enlaces con otros elementos.
De los átomos a las bandas de energía
Cuando los átomos se juntan para formar un sólido, los niveles de energía se combinan y aparecen grandes “bloques de departamentos”, que en física se conocen como bandas de energía, que se generan cuando dos átomos se acercan lo suficiente y sus orbitales se traslapan. En los sólidos cristalinos, los átomos están tan cercanos entre sí que los electrones de valencia constituyen un sistema único de electrones comunes en la estructura, generando dos bandas importantes: la banda de valencia que es donde se encuentran los electrones que mantienen unidos a los átomos y la banda de conducción que es donde los electrones pueden moverse libremente y transportar corriente.
Un electrón en la banda de valencia puede aumentar su energía y pasar hacia la banda de conducción, a fin de contribuir en la generación de corriente eléctrica y es gracias a este concepto que se puede comprender la capacidad conductiva de los materiales. Entre la banda de valencia y la banda de conducción puede haber un “espacio vacío” que los electrones no pueden cruzar tan fácilmente, conocida como banda prohibida, y es el espesor de este espacio el que puede determinar si un material es conductor, aislante o semiconductor.
La puerta de los conductores, aislantes y semiconductores
Metales como el cobre o la plata pueden ser pensados como una puerta abierta: si el espacio entre la banda de valencia y la banda de conducción es muy pequeño o si incluso las bandas se encuentran traslapadas, los electrones en la banda de valencia pasarán fácilmente hacia la banda de conducción y muchos podrán contribuir a la generación de corriente eléctrica; al igual que en una puerta abierta, los materiales conductores permiten el paso de los electrones.
Aislantes como el vidrio o la madera son como una puerta cerrada con candado: si el “espacio prohibido” entre la banda de valencia y la banda de conducción es muy grande, los electrones no pueden pasar hacia la banda de conducción y esto impide la generación de corriente eléctrica
Semiconductores como el silicio son como una puerta entreabierta: cuando el espacio entre la banda de valencia y la banda de conducción no es tan grande, con un pequeño empujón de luz o calor, los electrones pueden hacia la banda de conducción, y esa precisamente es la magia que hace que tengan la capacidad de comportarse como conductores o aislantes según se requiera.
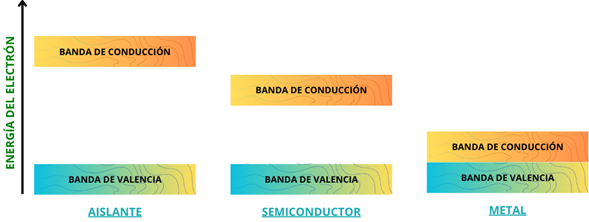
Figura 3. Diagrama de bandas de energía de materiales aislantes, semiconductores y metales.
La nueva generación de los materiales
Aunque el silicio es uno de los materiales más utilizados en la generación de dispositivos, los científicos realizan investigaciones para proponer nuevos materiales que presenten propiedades únicas para ser utilizados en la innovación tecnológica; algunos de estos materiales son:
Arsenuro de galio (GaAs): por sus características físicas y su estructura química, es un material ideal para aplicaciones electrónicas de alta frecuencia como radares y comunicaciones.
Disulfuro de molibdeno (MoS2): es un material con la capacidad de formar láminas delgadas, lo cual lo hace útil para la electrónica flexible.
Perovskitas hibridas: con materiales caracterizados por su alto rendimiento, conductividad y eficiencia en la absorción de luz.
Calcogenuros de antimonio (Sb2S3, Sb2Se3): son materiales económicos y abundantes que originan un bajo impacto ambiental; además, por su capacidad de absorción de luz son ideales para el diseño de celdas solares.
La investigación en nuevos materiales es necesaria para la generación de avances tecnológicos, ya que cada material tiene características únicas que podrían ser aprovechadas en el diseño de nuevos dispositivos como pantallas flexibles, paneles solares transparentes o computadoras avanzadas.
Aún hay un largo camino por recorrer, pero es un hecho que comprender las propiedades de los materiales ha contribuido al desarrollo de la ciencia y la tecnología, los metales con sus propiedades conductivas posibilitan su uso en la infraestructura eléctrica, los aislantes al no conducir electricidad garantizan la seguridad y el control de sistemas eléctricos y los semiconductores han revolucionado la electrónica debido a la capacidad que tienen de modificar su conductividad, de esta forma se puede comprender la razón por la cual los metales, los aislantes y los semiconductores son los protagonistas de una gran historia tecnológica.
Referencias
Acosta, V. (1975). El modelo de Bohr. En V. Acosta, Curso de Física Moderna (págs. 124-133). México: Oxford University Press.
Anuradha Saini, R. K. (2021). Introduction and brief history of thermoelectric materials. En R. Kumar, Thermoelectricity and Advanced Thermoelectric Materials (págs. 1-19). Chandigarh: Elsevier.
ChemTalk. (s.f.). Aufbau Principle. Obtenido de https://chemistrytalk.org/aufbau-principle/
Clark, J. (s.f.). Atomic Orbitals. Obtenido de https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_(Physical_and_Theoretical_Chemistry)/Electronic_Structure_of_Atoms_and_Molecules/Atomic_Orbitals
David M. Hanson, E. H. (2005). Bonding and Antibonding Orbitals. Quantum States of Atoms and Molecules.
Elmesery, M. (03 de 05 de 2025). The Power of Valence Electrons. Obtenido de https://praxilabs.com/en/blog/2024/03/14/the-role-of-valence-electrons/
El-Saba, M. H. (2014). Energy Band Theory & Classification of Solids. En M. E.-S. Lab, Electronic Engineering Materials & Nanotechnology (págs. 307-435). Egipto: Hakim Press.
Monique Combescot, O. B.-M. (2008). The many-body physics of composite bosons. Physics Reports, 215-320.
Ohring, M. (2002). Chapter 1 - A Review of Materials Science. En M. Ohring, Materials Science of Thin Films (págs. 1-56). New Jersey: Academic Press.
Quílez, J. (2025). Attempts to account for chemical periodicity in terms of the electronic structure of elements: Thomson, Bohr and Madelung. Foundations of Chemistry, 1-32.




Me parece un tema más que interesante y sobre todo completo para poder tener una base sobre la eléctricidad y la forma en que esta es conducida y utilizada para ciertas áreas, y dependiendo la aplicación así se utilizaran diferentes materiales que ayudaran a regular y mejorar el flujo de electricidad
1. La diferencia entre un material aislante y un semiconductor es que el aislante no permite de ninguna forma el paso de electrones a través de él, y el semiconductor puede actuar como aislante o como conductor según la condición en la que se encuentre.
2. Es un semiconductor compuesto ideal para la fabricación de dispositivos electrónicos de alta frecuencia, idealmente dispositivos de rastreo o comunicación.
Atentamente Noel Hernández.