Víctor Enrique Sarmiento-Ortega, Diana Moroni-González y Samuel Treviño
Palabras clave: Cadmio, Metabolismo, Toxicidad, Contaminación ambiental.
El cadmio (Cd) es un metal pesado de número atómico 48 y se encuentra en la tabla periódica en el grupo 12. Es un metal blanco-azulado, blando, con múltiples aplicaciones industriales, pero también con efectos perjudiciales para la salud.
El cadmio está presente de manera natural en el medio ambiente, se encuentra ampliamente distribuido en la corteza terrestre, generalmente como un subproducto de minerales que contienen zinc, plomo y cobre. Las condiciones ambientales de erosión transportan grandes cantidades del metal a través de los océanos, de esta forma los sedimentos oceánicos pueden contener concentraciones elevadas del metal descargándolos en ríos y lagos. Algunas plantas pueden absorber cadmio presente de manera natural en el suelo, lo que lo introduce en la cadena alimentaria. Debido a que está presente en la mayoría de los alimentos, la ingesta dietética es la principal fuente de exposición al Cd en la población. Además, las erupciones volcánicas pueden liberar altas concentraciones de Cd, las cuales son estimadas de entre 100 y 500 toneladas al año (Satarug et al., 2023).
Entre 1951 y 1980, la emisión antropogénica de cadmio superó ampliamente la natural, con un promedio de 8,000 toneladas anuales, contaminando principalmente suelos de cultivo e introduciéndose en la dieta humana y animal. Una fuente adicional de cadmio en las plantas es el uso de fertilizantes fosfatados, donde el metal está en forma iónica. También se encuentra en lechos de ríos debido a descargas industriales que contaminan suelos y mantos freáticos. La industria utiliza cadmio en aleaciones metálicas para mejorar la resistencia al desgaste y facilitar la fundición, además de reducir el punto de fusión. Sus pigmentos se emplean en tintes, pinturas, plásticos y cerámicas de colores brillantes (amarillo, naranja, rojo y marrón). También se usa en la fabricación de baterías de níquel-cadmio, conductores eléctricos, productos de PVC, fotoceldas, neumáticos, radiadores, componentes electrónicos y sistemas de calefacción (Cheng et al., 2014).
Los trabajadores de la industria relacionados con lo anteriormente descrito son los de mayor exposición a Cd; sin embargo, para la mayoría de la población, la exposición se produce principalmente al ingerir alimentos contaminados. Se ha estimado que más del 80% de la ingesta del metal proviene de cereales (especialmente arroz y trigo), verduras (especialmente de hoja verde) y tubérculos (especialmente papas y zanahorias), así como moluscos y crustáceos, los cuales pueden acumular altas concentraciones de Cd. Asimismo, el consumo de cigarro incrementa significativamente la cantidad de metal presente en el organismo, ya que se sabe que existen concentraciones alrededor de 1.5 μg de cadmio por cigarro. En general, los fumadores presentan niveles de Cd en sangre y en el cuerpo más del doble que los no fumadores (Satarug et al., 2023).
Las actividades antropogénicas han llevado a un aumento de la concentración de metales pesados en el medio ambiente, a pesar de que se han realizado considerables esfuerzos para controlar las emisiones al medio ambiente, la contaminación de los alimentos no se ha eliminado y se han demostrado problemas de salud, pese a lo anterior la contaminación atmosférica por Cd no está informada, ni monitoreada. Por lo tanto, las principales fuentes de exposición al Cd en humanos son la dieta, el agua contaminada, el aire contaminado y el humo del cigarrillo (Fatima et al., 2019).
El Cd es tóxico incluso en concentraciones bajas y puede causar efectos tanto agudos como crónicos en la salud. Una de sus características más peligrosas es su capacidad para acumularse en el organismo a lo largo de la vida (17 a 30 años). Diversos estudios indican que las principales fuentes de exposición al cadmio no laboral en la población general son los alimentos y el humo del cigarrillo. Los órganos más afectados por la toxicidad del cadmio incluyen los riñones, pulmones, huesos, sistema cardiovascular y nervioso. La exposición a altas concentraciones de cadmio se ha vinculado con enfermedades graves, particularmente en casos de intoxicación aguda o crónica en ambientes industriales. Se han registrado numerosos casos de envenenamiento por cadmio entre trabajadores industriales y comunidades expuestas a niveles elevados de contaminación (Das & Al-Naemi, 2019).
El Cd penetra en los organismos vivos a través del agua o los alimentos, en el intestino, el cadmio (Cd) es absorbido a través de transportadores de metales como Fe, Zn, Mn y Ca. Además, puede ingresar mediante transcitosis y endocitosis mediada por receptores en su forma unida a metalotioneína (Cd-MT) o fitoquelatinas (CdPC) de origen vegetal. Una vez absorbido, el Cd se transporta al hígado, donde estimula la síntesis de metalotioneína y forma complejos Cd-MT, que luego circulan en la sangre, se filtran en los riñones y son reabsorbidos por las células tubulares. En sangre, la mayor parte del Cd se encuentra en los eritrocitos. Como los riñones retienen la mayor parte del Cd, su acumulación en el cuerpo aumenta con la edad. La eliminación del Cd ocurre principalmente a través de la orina en forma de CdMT, aunque la mayor parte proviene de células tubulares dañadas. Los mecanismos de su toxicidad, como el estrés oxidativo, la inflamación y el daño celular, se han descrito a lo largo de los años, así como su relación con el desarrollo de diferentes enfermedades, estos casos suelen involucrar altas concentraciones (Thévenod & Lee, 2013).
Entre las principales enfermedades causadas por altas concentraciones a cadmio, se encuentran la Enfermedad de Itai-Itai, la cual ocurrió en Japón, debido a la contaminación del agua por residuos mineros, la cual se caracteriza por osteomalacia severa (huesos frágiles y dolorosos) y fallo renal. También puede generar daño renal severo (nefrotoxicidad) por acumulación en los riñones generando disfunción tubular renal, reduciendo la capacidad de los riñones para reabsorber proteínas, calcio y minerales en la orina. El daño Pulmonar por la inhalación de polvos y vapores de cadmio puede provocar enfermedad pulmonar obstructiva crónica (EPOC) y fibrosis pulmonar. Además, se ha relacionado con un mayor riesgo de cáncer de pulmón, principalmente en trabajadores expuestos a humos de cadmio (Charkiewicz et al., 2023).
Sin embargo, la exposición a bajas concentraciones de cadmio en el ambiente ha recibido menos atención científica, a pesar de sus posibles efectos acumulativos a largo plazo en la salud humana.
Cadmio y enfermedades metabólicas
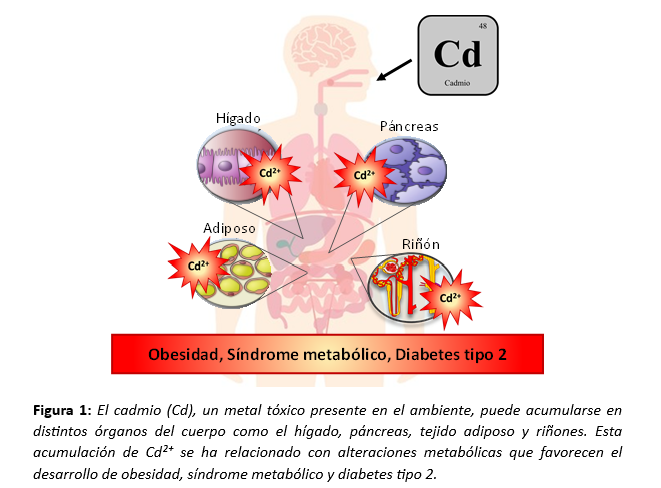
Estudios recientes sugieren que el cadmio a concentraciones de mínimo riesgo (valores que se usan para identificar exposiciones ambientales que no se esperan que dañen la salud) pueden generar una disrupción metabólica y el desarrollo de resistencia a insulina, hígado graso, obesidad, hipertensión y diabetes tipo 2. Como se muestra en la Figura 1, el cadmio afecta varios órganos clave en el desarrollo de estas enfermedades (Moroni-González et al., 2023).
Cadmio y daño pancreático
Después de la exposición a Cd en dosis definidas como no tóxicas, se ha mostrado que la exposición al cadmio causa un aumento sérico y acumulación del metal en el páncreas y los islotes de Langerhans e hiperglucemia asociadas con una alta producción de insulina. El cadmio aumenta la resistencia a la insulina en el hígado, el tejido adiposo y el sistema cardiovascular, mientras que los índices se sensibilidad a insulina se ven disminuidos (HOMA-S%, QUICKI y Matsuda-DeFronzo). Los grupos expuestos a Cd presentan altos niveles de especies reactivas de oxígeno (ROS) y peroxidación lipídica. Un aumento en las concentraciones de MT y Glutatión (GSH) con el aumento de la actividad enzimática del sistema glutatión, catalasa y superóxido dismutasa mantuvo un ambiente redox favorable, gracias a esto, los islotes de Langerhans muestran una alta tasa de supervivencia de las células de los islotes de Langerhans, así como hipertrofia celular, evitando así la muerte celular. Sin embargo, esta adaptación puede llevar a una hiperproducción de insulina, indicando un estado compensatorio de resistencia a la insulina (Moroni-González et al., 2024; Treviño et al., 2015).
Cadmio y resistencia hepática a insulina
Se ha informado que la exposición subaguda de una concentración de cadmio NOAEL (nivel sin efecto adverso observable) genera intolerancia a la glucosa, hiperinsulinemia, hiperleptinemia, inflamación y resistencia selectiva a la insulina en el hígado y el tejido adiposo. En el hígado, la síntesis de glucógeno disminuye, evento asociado al desarrollo de resistencia a insulina. Asimismo, que la exposición al Cd causa un aumento de ROS y del brazo miogénico de la señalización de la insulina, vía involucrada en procesos de crecimiento y proliferación. En el curso temporal de la exposición a estas dosis de cadmio se acentúa la producción de ROS disminuyendo crónicamente la defensa antioxidante, la sobreacumulación hepática de triglicéridos y las señales mitogénicas que desarrollan resistencia a la insulina. Finalmente, la inflamación y la peroxidación lipídica se presentan ante una exposición constante al Cd, mientras que la homeostasis de lípidos y carbohidratos se deteriora (Sarmiento-Ortega et al., 2022, 2023).
Cadmio e hígado graso y dislipidemia
La exposición a dosis LOAEL (nivel mínimo de efectos adversos observados) y NOAEL ha evidenciado un acumulo gradual importante en hígado. A nivel hepático la exposición a Cd a dosis ambientes altera la concentración de lípidos séricos y hepáticos. En hígado se incrementa considerablemente la concentración y el resguardo de colesterol y triglicéridos ya que la lipogénesis de novo aumenta debido a un incremento en la expresión de la proteína de unión al elemento regulador de esteroles 1c (SREBP-1c), factor de transcripción que regula la síntesis de lípidos y la homeostasis lipídica, lo cual genera un fenotipo similar el hígado graso no alcohólico. Además, se observa un incremento de la concentración de triglicéridos, colesterol total, colesterol LDL, colesterol VLDL y una disminución de colesterol HDL, además que se observa el desarrollo de LDL y HDL pequeñas ricas en triglicéridos, que favorecen un entorno aterogénico asociado a la dislipidemia (Sarmiento-Ortega et al., 2017, 2022).
Cadmio y obesidad
La exposición a dosis de mínimo riesgo de cadmio muestra un aumento en la concentración de Cd en el tejido adiposo de Cd, indicando que es un órgano blanco de su toxicidad. Se muestra un incremento en valores de peso, índice de masa corporal (IMC) y porcentaje de grasa, asociados a un incremento de la hipertrofia adipocítica. El balance redox se mantuvo debido al aumento de la expresión del factor nuclear eritroide 2 (Nrf2). Se observa un incremento en la concentración de la leptina, mientras que la adiponectina disminuyó (hormonas secretadas por el tejido adiposo metabólicamente importantes), indicando una disfunción del tejido. La resistencia a la insulina adiposa aumenta simultáneamente con la lipólisis y la intolerancia a la glucosa a pesar de la alta expresión del transportador de glucosa tipo 4 (GLUT4). Estos datos revelan que el cadmio genera un incremento de la obesidad, relacionado con disfunción del tejido adiposo estrechamente relacionada con inflamación y resistencia a la insulina (Sarmiento-Ortega et al., 2025).
Conclusiones
El cadmio, incluso en concentraciones ambientales, puede acumularse en tejidos clave como el páncreas, el hígado y el tejido adiposo, dependiendo de la dosis y vía de exposición. Esta acumulación se asocia con alteraciones metabólicas, incluyendo el síndrome metabólico. Aunque los mecanismos precisos aún no están completamente definidos, se reconoce que el estrés oxidativo y la inflamación desempeñan un papel importante en la progresión de enfermedades como la diabetes. Se plantea que la exposición al cadmio podría inducir cambios celulares adaptativos, como hipertrofia o hiperplasia, especialmente en el páncreas y tejido adiposo, afectando su función endocrina y promoviendo hiperinsulinemia, resistencia a la insulina y eventual disfunción celular. Además, la alteración en la secreción de adipocinas como leptina y adiponectina impacta negativamente en el equilibrio metabólico. Dada esta evidencia, el cadmio debe ser considerado un factor de riesgo en enfermedades metabólicas, y es esencial que futuros estudios se enfoquen en esclarecer los mecanismos moleculares implicados para desarrollar posibles estrategias terapéuticas.
Referencias
Charkiewicz, A. E., Omeljaniuk, W. J., Nowak, K., Garley, M., & Nikliński, J. (2023). Cadmium Toxicity and Health Effects—A Brief Summary. Molecules, 28(18), 6620. https://doi.org/10.3390/molecules28186620
Cheng, K., Tian, H. Z., Zhao, D., Lu, L., Wang, Y., Chen, J., Liu, X. G., Jia, W. X., & Huang, Z. (2014). Atmospheric emission inventory of cadmium from anthropogenic sources. International Journal of Environmental Science and Technology, 11(3), 605–616. https://doi.org/10.1007/s13762-013-0206-3
Das, S. C., & Al-Naemi, H. A. (2019). Cadmium Toxicity: Oxidative Stress, Inflammation and Tissue Injury. Occupational Diseases and Environmental Medicine, 07(04), 144–163. https://doi.org/10.4236/odem.2019.74012
Fatima, G., Raza, A. M., Hadi, N., Nigam, N., & Mahdi, A. A. (2019). Cadmium in Human Diseases: It’s More than Just a Mere Metal. Indian Journal of Clinical Biochemistry, 34(4), 371–378. https://doi.org/10.1007/s12291-019-00839-8
Moroni-González, D., Sarmiento-Ortega, V. E., Diaz, A., Brambila, E., & Treviño, S. (2023). Pancreas–Liver–Adipose Axis: Target of Environmental Cadmium Exposure Linked to Metabolic Diseases. Toxics, 11(3), 223. https://doi.org/10.3390/toxics11030223
Moroni-González, D., Sarmiento-Ortega, V. E., Diaz, A., Brambila, E., & Treviño, S. (2024). Pancreatic Antioxidative Defense and Heat Shock Proteins Prevent Islet of Langerhans Cell Death After Chronic Oral Exposure to Cadmium LOAEL Dose. Biological Trace Element Research, 202(8), 3714–3730. https://doi.org/10.1007/s12011-023-03955-y
Sarmiento-Ortega, V. E., Alcántara-Jara, D. I., Moroni-González, D., Diaz, A., Vázquez-Roque, R. A., Brambila, E., & Treviño, S. (2025). Chronic cadmium exposure to minimal-risk doses causes dysfunction of epididymal adipose tissue and metabolic disorders. Toxicology and Applied Pharmacology, 495, 117203. https://doi.org/10.1016/j.taap.2024.117203
Sarmiento-Ortega, V. E., Moroni-González, D., Diaz, A., Brambila, E., & Treviño, S. (2023). ROS and ERK Pathway Mechanistic Approach on Hepatic Insulin Resistance After Chronic Oral Exposure to Cadmium NOAEL Dose. Biological Trace Element Research, 201(8), 3903–3918. https://doi.org/10.1007/s12011-022-03471-5
Sarmiento-Ortega, V. E., Moroni-González, D., Díaz, A., Eduardo, B., & Samuel, T. (2022). Oral Subacute Exposure to Cadmium LOAEL Dose Induces Insulin Resistance and Impairment of the Hormonal and Metabolic Liver-Adipose Axis in Wistar Rats. Biological Trace Element Research, 200(10), 4370–4384. https://doi.org/10.1007/s12011-021-03027-z
Sarmiento-Ortega, V. E., Treviño, S., Flores-Hernández, J. Á., Aguilar-Alonso, P., Moroni-González, D., Aburto-Luna, V., Diaz, A., & Brambila, E. (2017). Changes on serum and hepatic lipidome after a chronic cadmium exposure in Wistar rats. Archives of Biochemistry and Biophysics, 635, 52–59. https://doi.org/10.1016/j.abb.2017.10.003
Satarug, S., Vesey, D. A., Gobe, G. C., & Phelps, K. R. (2023). Estimation of health risks associated with dietary cadmium exposure. Archives of Toxicology, 97(2), 329–358. https://doi.org/10.1007/s00204-022-03432-w
Thévenod, F., & Lee, W.-K. (2013). Toxicology of Cadmium and Its Damage to Mammalian Organs (pp. 415–490). https://doi.org/10.1007/978-94-007-5179-8_14
Treviño, S., Waalkes, M. P., Flores Hernández, J. A., León-Chavez, B. A., Aguilar-Alonso, P., & Brambila, E. (2015). Chronic cadmium exposure in rats produces pancreatic impairment and insulin resistance in multiple peripheral tissues. Archives of Biochemistry and Biophysics, 583, 27–35. https://doi.org/10.1016/j.abb.2015.07.010